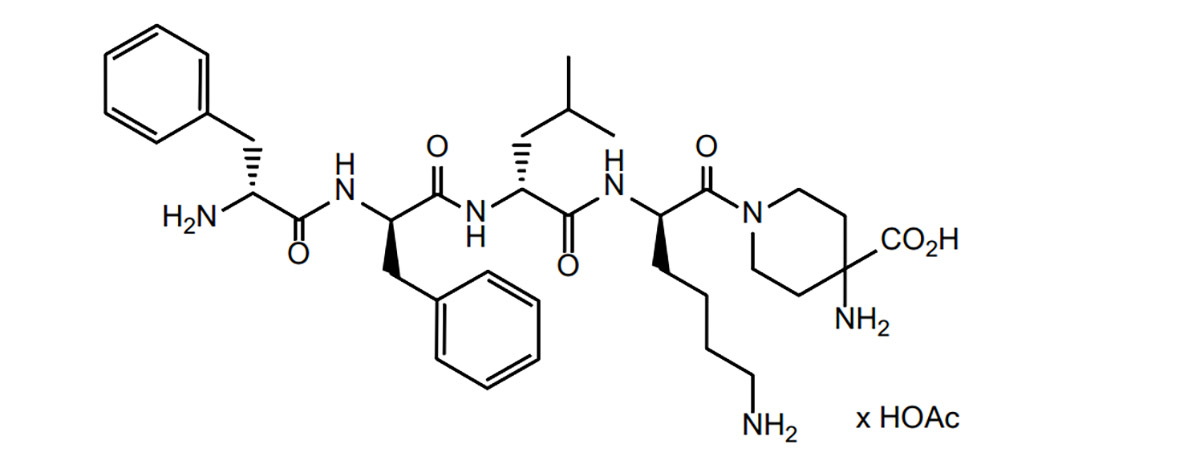
Již 24. srpna 2021 společnost Cara Therapeutics a její obchodní partner Vifor Pharma oznámily, že její první agonista kappa opioidních receptorů difelikefalin (KORSUVA™) byl schválen Úřadem pro kontrolu potravin a léčiv (FDA) pro léčbu pacientů s chronickým onemocněním ledvin (CKD) (pozitivní středně těžké/těžké svědění s hemodialýzou). Jeho uvedení na trh se očekává v prvním čtvrtletí roku 2022. Společnosti Cara a Vifor podepsaly exkluzivní licenční smlouvu na komercializaci přípravku KORSUVA™ ve Spojených státech a dohodly se na prodeji přípravku KORSUVA™ společnosti Fresenius Medical. Společnosti Cara a Vifor mají každá 60% a 40% podíl na tržbách z prodeje kromě společnosti Fresenius Medical; každá má 50% podíl na tržbách z prodeje společnosti Fresenius Medical.
Svědění spojené s chronickým onemocněním ledvin (CKD-aP) je generalizované svědění, které se vyskytuje s vysokou frekvencí a intenzitou u pacientů s CKD podstupujících dialýzu. Svědění se vyskytuje u přibližně 60–70 % pacientů podstupujících dialýzu, z nichž 30–40 % má středně těžké/těžké svědění, které závažně ovlivňuje kvalitu života (např. špatnou kvalitu spánku) a je spojeno s depresí. Dosud neexistuje účinná léčba svědění souvisejícího s CKD a schválení přípravku Difelikefalin pomáhá řešit obrovskou mezeru v potřebě lékařské péče. Toto schválení je založeno na dvou klíčových klinických studiích fáze III, které jsou součástí žádosti o NDA: pozitivních datech ze studií KALM-1 a KALM-2 v USA a celosvětově a podpůrných datech z 32 dalších klinických studií, které prokazují, že přípravek KORSUVA™ je dobře snášen.
Nedávno přišly dobré zprávy z klinické studie difelikefalinu v Japonsku: 10. ledna 2022 společnost Cara oznámila, že její partneři Maruishi Pharma a Kissey Pharma potvrdili, že injekce difelikefalinu se v Japonsku používá k léčbě svědění u pacientů na hemodialýze. Klinické studie fáze III Primární cílový parametr byl splněn. 178 pacientů dostávalo 6 týdnů difelikefalinu nebo placeba a zúčastnilo se 52týdenní otevřené prodloužené studie. Primární cílový parametr (změna skóre numerické stupnice hodnocení svědění) a sekundární cílový parametr (změna skóre svědění na Shiratoriho stupnici závažnosti) se ve skupině s difelikefalinem ve srovnání se skupinou s placebem významně zlepšily oproti výchozímu stavu a pacienti byli dobře tolerováni.
Difelikefalin je třída opioidních peptidů. Na tomto základě Peptidový výzkumný ústav prostudoval literaturu o opioidních peptidech a shrnul obtíže a strategie opioidních peptidů ve vývoji léčiv, jakož i současnou situaci v oblasti vývoje léčiv.
Čas zveřejnění: 17. února 2022